Transtiretin Kardiyak Amiloidozu Değerlendirme ve Yönetim:
2025 ACC Kısa Klinik Rehberi
Kittleson et al JACC VOL. 87, NO. 5, 2026
Transtiretin amiloid kardiyomiyopatisi, özellikle ileri yaştaki bireylerde giderek daha sık tanınan bir kalp yetersizliği nedeni olarak ortaya çıkmıştır. Günümüzde, özellikle bilateral karpal tünel sendromu veya spinal stenoz gibi kas-iskelet sistemi bulguları bulunan bireylerde, kalp yetersizliğinin altta yatan etiyolojisi olarak transtiretin amiloid kardiyomiyopatisine yönelik farkındalık artmıştır. Tanı alanında da önemli ilerlemeler kaydedilmiştir; özellikle monoklonal protein taraması negatif olan bireylerde radyonüklid sintigrafi kullanılarak doğru ve noninvaziv tanı koyabilme olanağı bunlar arasındadır. Son olarak, transtiretin amiloid kardiyomiyopatisi olan bireyler; mineralokortikoid reseptör antagonistleri ve sodyum-glukoz kotransporter 2 inhibitörleri gibi geniş ölçüde etkili kalp yetersizliği tedavilerinin yanı sıra, transtiretin stabilizatörleri olan tafamidis ve akoramidis ile transtiretin baskılayıcısı vutrisiran gibi hastalığa özgü, hastalık modifiye edici tedavilerden de yarar görmüştür. Bu Kısa Klinik Rehber’in amacı, genişleyen tedavi seçeneklerini yansıtacak şekilde klinisyenlere güncellenmiş stratejiler sunmak ve özellikle hastalık modifiye edici tedavi seçimi, kalp yetersizliği tedavileri ve geleceğe yönelik yaklaşımlar üzerine odaklanarak transtiretin amiloid kardiyomiyopatisinin tanı ve yönetiminde en iyi uygulamaları pekiştirmektir.
1. GİRİŞ
Transtiretin amiloid kardiyomiyopatisi (ATTR-CM), özellikle ileri yaştaki bireylerde giderek daha sık tanınan bir kalp yetersizliği (KY) nedeni olarak ortaya çıkmıştır. Günümüzde ATTR-CM’nin KY’nin altta yatan bir nedeni¹ ve aort darlığı ile eşlik eden bir tanı² olduğu konusunda farkındalık artmıştır; özellikle bilateral karpal tünel sendromu³ veya spinal stenoz⁴ gibi kas-iskelet sistemi bulguları bulunan bireylerde bu durum daha belirgindir. Tanı alanında önemli ilerlemeler kaydedilmiştir; bunlar arasında, monoklonal protein taraması negatif olan bireylerde radyonüklid sintigrafi kullanılarak doğru ve noninvaziv tanı koyabilme olanağı da bulunmaktadır⁵. Son olarak, ATTR-CM’li bireyler etkili KY tedavilerindeki gelişmelerden yarar görmüştür; bunlar arasında mineralokortikoid reseptör antagonistleri⁶⁻⁸ ve sodyum-glukoz kotransporter 2 inhibitörleri⁷⁻⁹ ile birlikte, transtiretin stabilizatörleri tafamidis¹⁰ ve akoramidis¹¹ ile transtiretin baskılayıcısı vutrisiran¹² gibi hastalık modifiye edici tedaviler yer almaktadır.
Bu Kısa Klinik Rehber’in (CCG) amacı, genişleyen tedavi seçeneklerini yansıtacak şekilde klinisyenlere güncellenmiş stratejiler sunmak ve özellikle hastalık modifiye edici tedavi seçimi, geleceğe yönelik yaklaşımlar ve yanıtlanmamış sorulara odaklanarak ATTR-CM’nin tanı ve yönetiminde en iyi uygulamaları pekiştirmektir.
Tanımlamalar;
- GDMT (Kılavuzlara Dayalı Medikal Tedavi): Klinik uygulama kılavuzları tarafından kullanımına destek verilen ve ATTR-CM’li bireylerde kullanımına ilişkin özel hususları içeren tedavi seçeneklerini ifade eder.
- KY (Kalp Yetersizliği): “2022 AHA/ACC/HFSA Kalp Yetersizliği Yönetim Kılavuzu”nda belirtilen kriterlere göre tanımlanır.¹³ Hastaneye yatış dahil olmak üzere bir KY olayı, “2014 ACC/AHA Klinik Çalışmalarda Kardiyovasküler Sonlanım Olayları için Temel Veri Elemanları ve Tanımlar” belgesinde belirtilen kriterlere göre tanımlanır.¹⁴
- Azalmış ejeksiyon fraksiyonlu kalp yetersizliği (HFrEF): Klinik KY tanısı ve sol ventrikül ejeksiyon fraksiyonu ≤%40.¹³
- Hafif derecede azalmış ejeksiyon fraksiyonlu kalp yetersizliği (HFmrEF): Klinik KY tanısı ve sol ventrikül ejeksiyon fraksiyonu %41–49.¹³
- Korunmuş ejeksiyon fraksiyonlu kalp yetersizliği (HFpEF): Klinik KY tanısı ve sol ventrikül ejeksiyon fraksiyonu ≥%50.¹³
- Monoklonal protein taraması: Serum kappa ve lambda serbest hafif zincir oranında anormallik veya serum immünfiksasyon elektroforezinde ya da idrar immünfiksasyon elektroforezinde monoklonal bant varlığı. Bu testler birlikte değerlendirildiğinde AL amiloidozunun saptanmasında >%99 duyarlılığa sahiptir.¹⁵
New York Kalp Derneği (NYHA) fonksiyonel sınıflaması:
- Sınıf I: Fiziksel aktivitede kısıtlılık yoktur. Olağan fiziksel aktivite KY semptomlarına yol açmaz.
- Sınıf II: Fiziksel aktivitede hafif kısıtlılık vardır. İstirahatte rahattır; ancak olağan fiziksel aktivite KY semptomlarına neden olur.
- Sınıf III: Fiziksel aktivitede belirgin kısıtlılık vardır. İstirahatte rahattır; ancak olağandan daha az düzeyde aktivite bile KY semptomlarına yol açar.
- Sınıf IV: KY semptomları olmaksızın herhangi bir fiziksel aktiviteyi gerçekleştiremez veya istirahatte de KY semptomları mevcuttur.
Kısaltmalar
- ATTR-CM = transtiretin kardiyomiyopatisi
- ATTRv-CM = varyant (mutant) transtiretin amiloid kardiyomiyopatisi
- ATTRwt-CM = vahşi tip (wild-type) transtiretin amiloid kardiyomiyopatisi
- eGFR = tahmini glomerüler filtrasyon hızı
- HF = kalp yetersizliği
- HFmrEF = hafif derecede azalmış ejeksiyon fraksiyonlu kalp yetersizliği
- HFpEF = korunmuş ejeksiyon fraksiyonlu kalp yetersizliği
- HFSA = Amerika Kalp Yetersizliği Derneği
- MRA = mineralokortikoid reseptör antagonisti
- NYHA = New York Kalp Derneği
- SGLT2 = sodyum-glukoz kotransporter-2
TANIM, GEREKÇE VE KLİNİK SONUÇLAR
Tanı
Klinik İpuçları
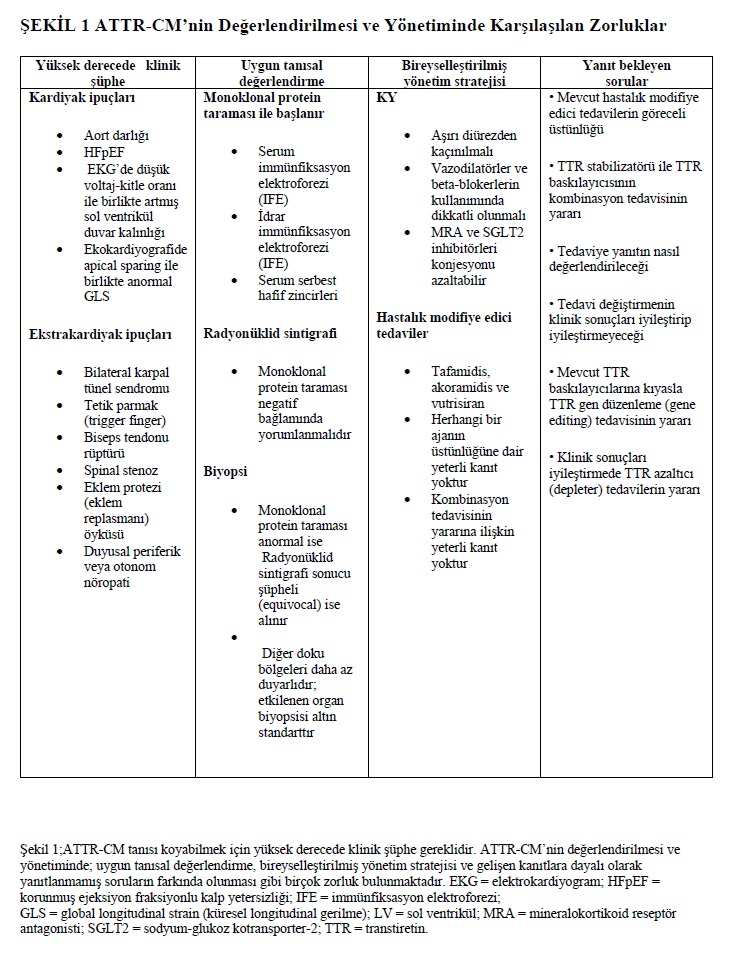
Kardiyak amiloidoz, yeterince tanınmayan bir durumdur ve bu nedenle tanı koyabilmek için yüksek derecede klinik şüphe gerektirir (Tablo 1). Klinik prezentasyon heterojen ve nonspesifiktir; sıklıkla yaşa bağlı daha yaygın kardiyak durumları taklit eder. Dejeneratif aort kapak darlığı olan hastaların² veya HFpEF’li hastaların¹˒¹⁶˒¹⁷ yaklaşık %15’inde ATTR birikimi gözlenmektedir.
Ekstrakardiyak transtiretin amiloid birikimi, genellikle yumuşak dokularda olup, çoğu zaman kardiyak tutulumdan önce ortaya çıkar; ATTR-CM’li bireylerin yaklaşık %80’inde omuz, kalça veya diz cerrahisi; karpal tünel sendromu; spinal stenoz; tetik parmak; ya da biseps tendonu rüptürü gibi ortopedik girişimler öyküsü mevcuttur¹⁸. Ligamentum flavum’da transtiretin birikimi, lomber spinal stenoz nedeniyle ameliyat edilen ileri yaştaki bireylerin üçte birine kadarında bildirilmiştir¹⁹˒²⁰. Spontan biseps tendonu rüptürü, kalp yetersizliği tanısından ortalama 5 yıl önce ortaya çıkabilir²¹; karpal tünel sendromu ise kardiyak tanıdan 5–10 yıl önce görülebilir²²˒²³. Bununla birlikte, kas-iskelet sisteminde transtiretin amiloid birikimi kanıtı bulunan bireylerin ne kadarının sonunda kardiyak bulgular geliştireceği tam olarak aydınlatılmamıştır. Polinöropati, özellikle periferik duyusal veya otonomik disfonksiyon şeklinde, ATTR’de görülebilir. ATTRv’de periferik nöropati varlığı varyanta göre değişkenlik gösterir. Portekiz’in endemik bölgelerinde p.Val50Met varyantına sahip bireylerin >%80’i 50 yaşına kadar periferik nöropati geliştirir. Buna karşılık, ağırlıklı olarak kardiyomiyopati ile ilişkili olan p.Val142Ile varyantında polinöropati prevalansı yaklaşık %10’dur. ATTRwt ise çoğunlukla kardiyomiyopatiye neden olur; hastaların yaklaşık %30’unda polinöropati bulunabilir ve bu durum amiloidoza bağlı olabilir ya da olmayabilir²⁴⁻²⁶.
Elektrokardiyografi, ekokardiyografi ve kardiyak manyetik rezonans (CMR) görüntüleme tanıyı düşündürebilir (Tablo 1). AL amiloidozunun aksine, elektrokardiyogramda (EKG) düşük QRS voltajı ATTR-CM için duyarlı değildir ve olguların yalnızca %25–40’ında gözlenir. Daha doğru bir elektrokardiyografik parametre voltaj/kitle oranıdır²⁷˒²⁸. Ekokardiyografi, artmış sol ventrikül duvar kalınlığı ve sıklıkla apikal korunma paterni ile birlikte anormal global longitudinal strain (GLS) gösterir²⁹⁻³¹. CMR’de geç gadolinyum tutulumu ve ekstrasellüler hacim ölçümü tamamlayıcı bilgiler sağlar³²; Ancak ne ekokardiyografi ne de CMR, doku biyopsisi olmaksızın ATTR-CM tanısını kesin olarak koydurabilir ya da ATTR-CM’yi AL amiloidozundan güvenilir biçimde ayırt edebilir. Kardiyak biyobelirteçler, klinik şüphesi düşük olan bireylerde ATTR-CM’yi dışlamak için yardımcı araçlar olarak kullanılabilir; N-terminal pro–B-tipi natriüretik peptid (NT-proBNP) <180 ng/L ve yüksek duyarlılıklı troponin T (hs-TnT) <14 ng/L eşik değerleri ATTR-CM’yi dışlayabilir³³˒³⁴. Kardiyak ve nonkardiyak klinik ipuçlarının ATTR-CM için pretest olasılığına nasıl dönüştürüleceğine ilişkin kanıta dayalı yerleşik bir algoritma bulunmamakla birlikte; yaş, cinsiyet, hipertansiyon tanısı, relatif duvar kalınlığı, posterior duvar kalınlığı ve ejeksiyon fraksiyonunu içeren 6 değişkenli bir skor bildirilmiş olup, tarama aracı olarak yol gösterici olabilir³⁵. EKG³⁶, ekokardiyografi³⁷ ve kardiyak MR³⁸ için geliştirilen yapay zekâ ve makine öğrenimi temelli tarama algoritmaları, ATTR-CM tanısında ortaya çıkan yeni araçlardır. Ayrıca, tanısal algoritmanın başlatılmasını gerektiren yüksek getirili klinik ve görüntüleme ipuçlarının özeti Tablo 1’de sunulmaktadır.
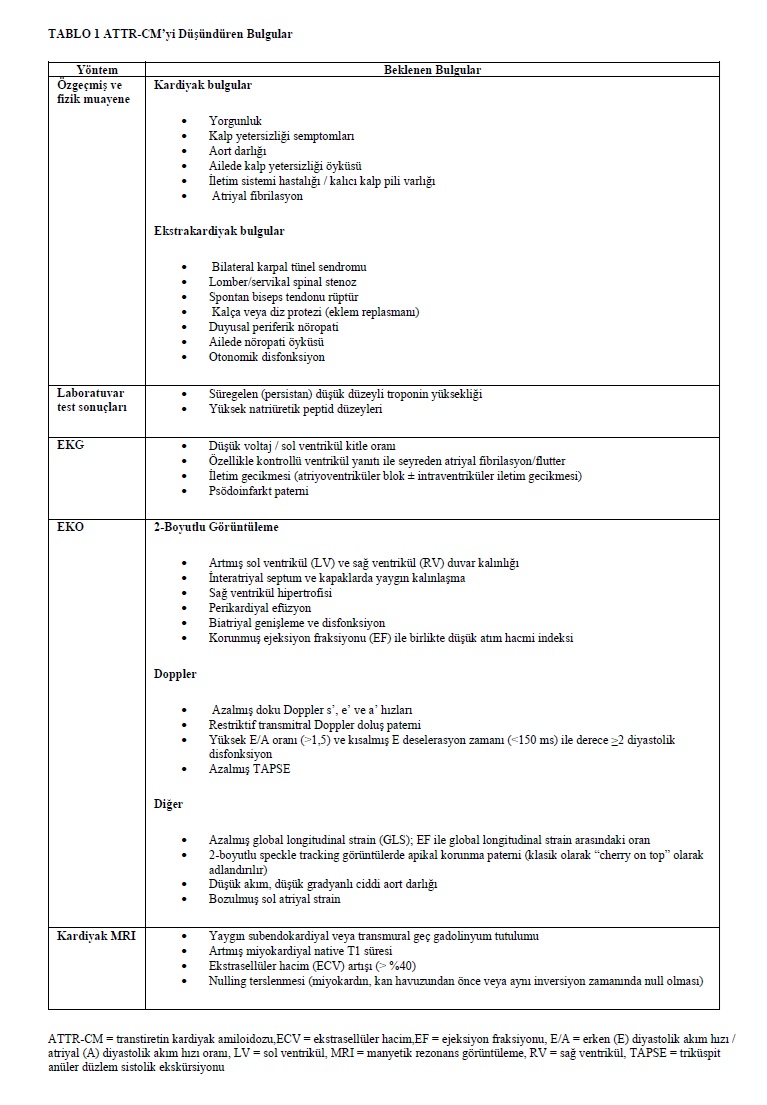
4.1.2. Tanısal Algoritma
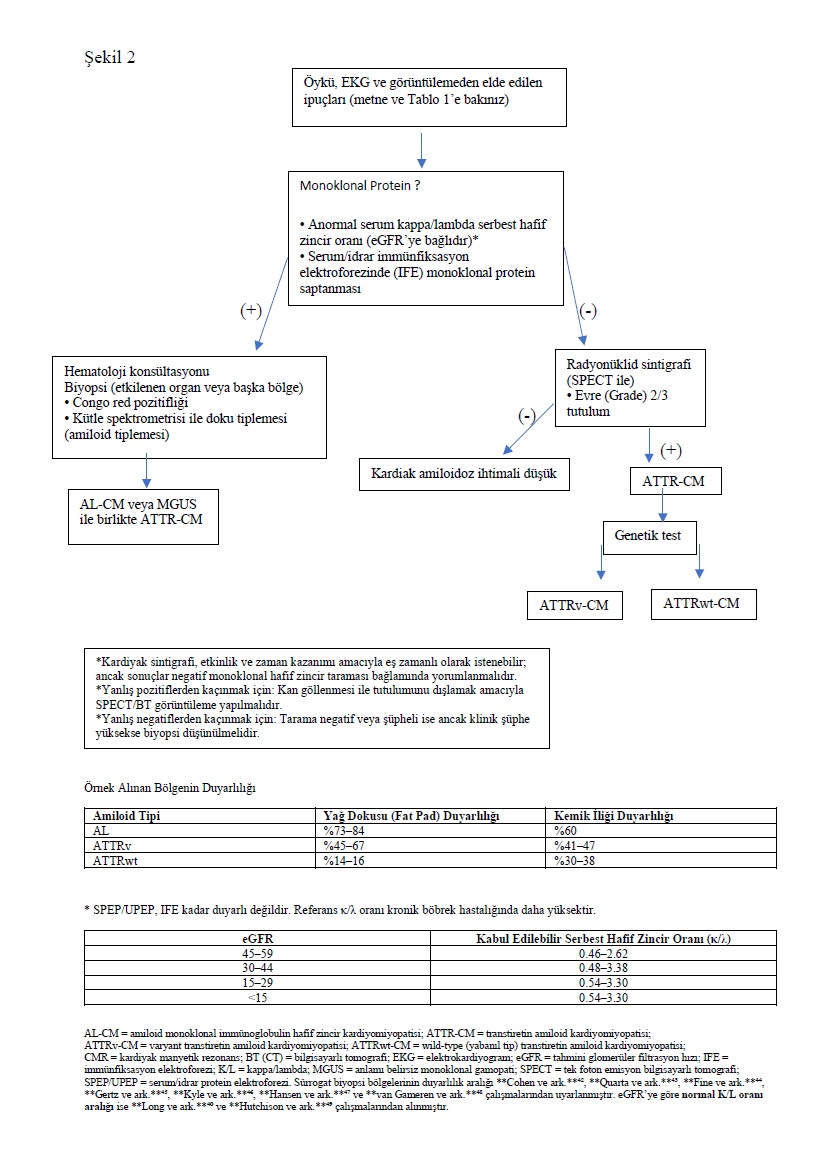
ATTR-CM’nin tanısal değerlendirmesindeki ilk ve en kritik adım, hafif zincir (AL) amiloidozunun dışlanmasıdır (Şekil 2). Bu amaçla serum serbest hafif zincir analizi ile birlikte serum ve idrar elektroforezi ve immünfiksasyon yapılır; bu üç testin kombinasyonu AL amiloidozunun saptanmasında %99 duyarlılığa sahiptir.39 Tanısal amaçla mutlak düzeylerden ziyade kappa ve lambda serbest hafif zincir oranı kullanılmalıdır. Özellikle, böbrek fonksiyon bozukluğu kappa hafif zincirlerinin renal klirensinin azalmasına bağlı olarak beklenenden daha yüksek kappa/lambda oranına yol açabileceğinden, bu oran böbrek fonksiyon bozukluğundan etkilenir. Bu gibi durumlarda serum ve idrar immünfiksasyon elektroforezi sonuçları genellikle normaldir ve AL amiloidozu nadirdir (Şekil 2).40 Ancak lambda serbest hafif zincir düzeylerinin artmasına bağlı olarak kappa/lambda oranının düşmesi durumunda ileri inceleme yapılmalıdır. Anormal monoklonal protein taramasının yorumlanması konusunda belirsizlik varsa, plazma hücre diskrazisinin varlığını doğrulamak amacıyla ileri tetkik gereksinimini belirlemek için bir hematoloji uzmanına danışılması yararlı olabilir.41 AL amiloidozu, negatif monoklonal protein taraması ile dışlandıktan sonra, noninvaziv tanı için radyonüklid sintigrafi kullanılabilir. Monoklonal protein yokluğunda Perugini evre 2 veya 3 miyokardiyal radyotracer tutulumu, ATTR-CM için %100 pozitif prediktif değere sahiptir.5 Ancak monoklonal protein taraması anormal olan her bireyde kesin tanı için doku biyopsisi ve kütle spektrometrisi ile amiloid tiplemesi yapılmalıdır.
4.1.3. Tanısal Hatalar
Sık görülen tanı hatalarından kaçınmak için dikkatli olunmalıdır. Kardiyak amiloidoz şüphesi olan ve monoklonal protein taraması anormal bulunan bireylerde, tutulum olan organ dışı bölgeden (örneğin abdominal yağ veya kemik iliği) biyopsi alınması düşük duyarlılığa sahiptir (Şekil 2).⁴²⁻⁴⁴ Bu nedenle, pozitif olduğunda yardımcı olmakla birlikte, negatif yağ doku biyopsisi sonucu ne AL amiloid kardiyomiyopatisini ne de ATTR-CM’yi dışlar; tanıyı kesinleştirmek için etkilenmiş bir organdan biyopsi gerekebilir. ATTR-CM’nin biyopsisiz tanısında, standartlaştırılmış radyonüklid görüntüleme protokollerine sıkı şekilde uyulması esastır.²⁹ 99m Teknesyum (⁹⁹ᵐTc) ile işaretli kemik-tutucu bileşikler (pirofosfat dahil), DPD (3,3-difosfono-1,2-propanodikarboksilik asit) ve HDP (hidroksimetilen difosfonat) kullanılır. Pirofosfat tarihsel olarak Amerika Birleşik Devletleri’nde kullanılmaktadır; ancak pirofosfat yokluğu durumunda tanısal gecikmeleri önlemek amacıyla veya alternatif bir görüntüleme ajanı olarak HDP kullanılabilir.⁵⁰
Planar görüntülemede görülen diffüz miyokardiyal tutulum, yanlış sınıflandırmayı önlemek amacıyla radyotraser enjeksiyonundan 2–3 saat sonra yapılan tek foton emisyon bilgisayarlı tomografi (SPECT) veya SPECT/bilgisayarlı tomografi (SPECT/BT) görüntüleme teknikleri kullanılarak kan göllenmesine bağlı aktiviteden ayırt edilmelidir.⁵¹
Yanlış pozitif sintigrafi taramasının diğer nedenleri arasında önceden geçirilmiş miyokard enfarktüsü, kalp üzerine projekte olan kaburga kırıkları, hidroksiklorokin toksisitesi ve AL amiloidozu yer alır. Buna karşılık, yanlış negatif taramalar bazı ATTR varyantlarına sahip bireylerde (p.Phe84Leu ve p.Val50Met) veya hastalığın erken evrelerinde görüle bilir.
4.2. Tedavi
4.2.1. Hastalığı Değiştirici Tedavilere Genel Bakış
4.2.1.1. Transtiretin Stabilizatörleri
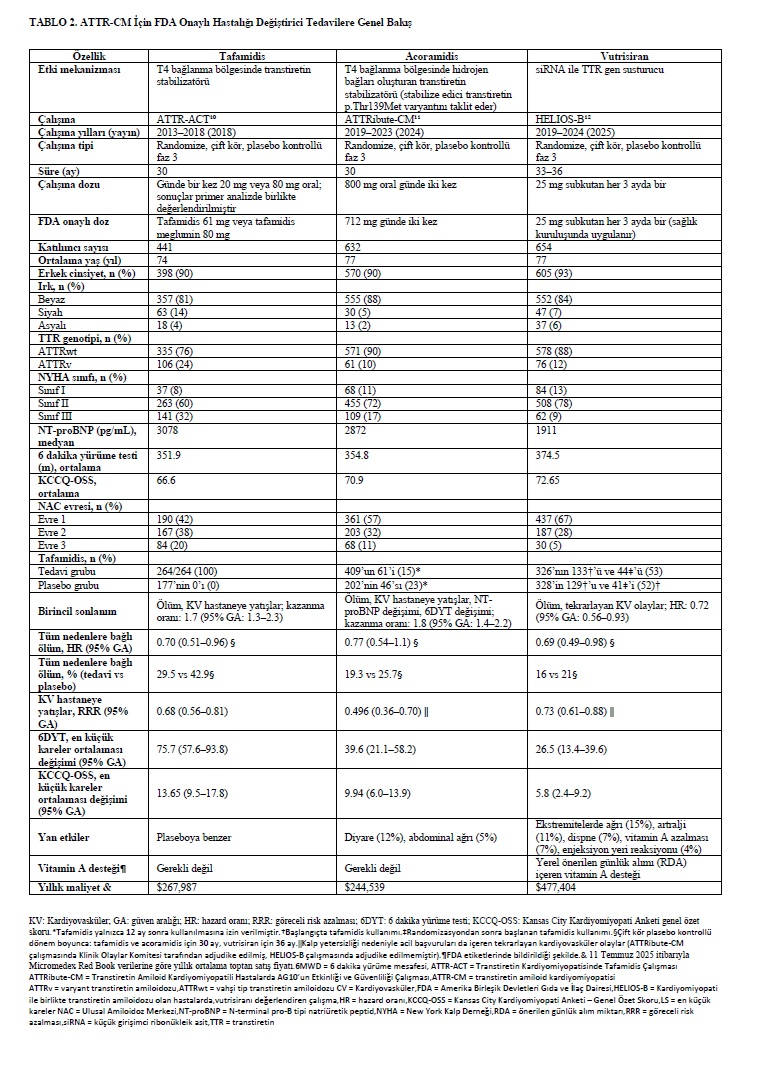
Transtiretin stabilizatörleri, transtiretinin normal tetramerik yapısını koruyarak onun ayrışmasını, yanlış katlanmasını ve dokularda biriken amiloid fibrillerine agregasyonunu önler. 2019 yılında tafamidis, ATTR-CM için ABD Gıda ve İlaç Dairesi (FDA) tarafından onaylanan ilk transtiretin stabilizatörü olmuştur. Bu onay, ATTR-CM’li 441 bireyin tafamidis veya plaseboya randomize edildiği ATTR-ACT (Tafamidis in Transthyretin Cardiomyopathy Clinical Trial) çalışmasının sonuçlarına dayanmaktadır. ¹⁰ 30 ayın sonunda, tafamidis tüm nedenlere bağlı mortaliteyi ve kardiyovasküler nedenli hastaneye yatış sıklığını azaltmıştır (Tablo 2). Uzun dönem uzatma çalışmasında, medyan 51 aylık takipte, 80 mg dozunun 20 mg’a kıyasla ölüm riskinde %30 relatif azalma sağladığı gösterilmiştir. ⁵² Tafamidis 61 mg serbest asit, tafamidis meglumin 80 mg’a (4 × 20 mg) biyoeşdeğerdir. ⁵³ Bu iki formun her ikisi de ATTR-CM için FDA tarafından onaylanmıştır. Tafamidis genellikle iyi tolere edilse de, rabdomiyoliz riski nedeniyle rosuvastatin >20 mg veya atorvastatin >40 mg ile birlikte kullanılırken dikkatli olunmalıdır. Acoramidis de bir başka transtiretin stabilizatörüdür.⁵⁴ 2024 yılında, ATTRibute-CM (Efficacy and Safety of AG10 in Subjects With Transthyretin Amyloid Cardiomyopathy) klinik çalışmasının sonuçlarının ardından FDA tarafından onaylanmıştır.¹¹˒⁵⁵˒⁵⁶ Bu çalışmada 632 ATTR-CM hastasında, günde iki kez 800 mg acoramidis hidroklorür ile plasebo karşılaştırılmıştır.¹¹ 30 aylık takip sonunda, acoramidis tüm nedenlere bağlı mortalite ve kardiyovasküler hastaneye yatışlar üzerinde olumlu etki göstermiştir.¹¹˒⁵⁵˒⁵⁶ (Tablo 2) FDA tarafından onaylanan doz günde iki kez oral 712 mg’dır (bu doz 800 mg acoramidis hidroklorüre eşdeğerdir).
4.2.1.2. Transtiretin Susturucuları (Transthyretin Silencers)
Transtiretin susturucuları, hepatositlerde transtiretin mesajcı ribonükleik asidinin (mRNA) yıkımına neden olarak transtiretin üretimini azaltır. 57 Amiloidoz için incelenen iki gen susturucu yaklaşım türü, küçük girişimci ribonükleik asitler (small-interfering RNA) ve antisens oligonükleotidlerdir.
Vutrisiran, 2022 yılında polinöropatili kalıtsal transtiretin amiloidozu (ATTRv) için ABD Gıda ve İlaç Dairesi (FDA) tarafından onaylanmıştır; ATTR-CM için onayı ise 2025 yılında gerçekleşmiştir. HELIOS-B (Transtiretin Amiloidozuna Bağlı Kardiyomiyopatili Hastalarda Vutrisiranın Değerlendirildiği Bir Çalışma) çalışmasında, 655 bireyde 12 haftada bir 25 mg subkutan vutrisiran ile plasebo karşılaştırılmıştır. 12 Vutrisiran tedavisi, tüm nedenlere bağlı ölüm ve tekrarlayan kardiyovasküler olaylar riskinde daha düşük oranlarla ilişkili bulunmuştur (Tablo 2). Transtiretin, retinolün başlıca taşıyıcısı olduğundan, dolaşımdaki transtiretin üretimini azaltan herhangi bir tedavi sırasında A vitamini takviyesi önerilmektedir. FDA tarafından onaylanan vutrisiran dozu, her 3 ayda bir 25 mg subkutan uygulama ve eş zamanlı A vitamini desteğidir.
4.2.2. Hastalık Modifiye Edici Tedaviler Arasında Seçim
4.2.2.1. ATTR-CM Hastalık Modifiye Edici Tedaviler İçin Uygun Bireylerin Seçilmesi
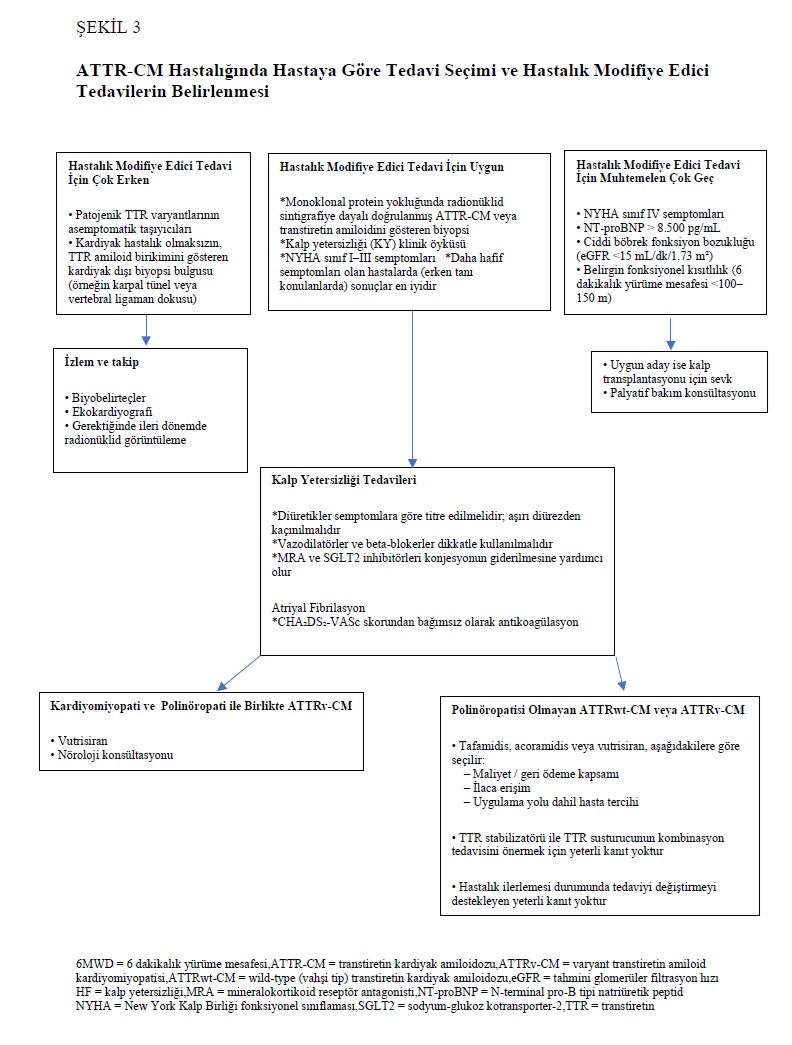
Etki mekanizmaları gereği, transtiretin stabilizatörleri olan tafamidis ve acoramidis ile transtiretin susturucusu vutrisiran hastalığın ilerlemesini yavaşlatır; ancak hedef organ hasarını geri döndürmez. Bu nedenle bu tedavilerin, fonksiyonel durumu ve yaşam kalitesini iyileştirmekten ziyade koruması beklenir. ATTR-CM için hastalık modifiye edici tedaviye başlamak için en uygun zaman, belirgin hedef organ disfonksiyonu gelişmeden önce semptomatik hastalığın en erken başlangıcıdır (Şekil 3).
Patolojik TTR varyantlarının asemptomatik taşıyıcılarının taranması veya kardiyak tutulum kanıtı olmayan kardiyak dışı transtiretin amiloidozu bulunan bireylerin değerlendirilmesi ve ayrıca ATTR-CM’de aritmilerin yönetimi ile ilgili ayrıntılar için Kittleson ve ark.41 çalışmasına bakınız. Genel olarak ATTR-CM için hastalık modifiye edici tedaviye uygun bireyler, temel klinik çalışmaların kriterlerine göre seçilmelidir. Doğrulanmış ATTR-CM tanısı ve NYHA sınıf I-III semptomları ile seyreden semptomatik kalp yetersizliği; buna kalp yetersizliği nedeniyle hastaneye yatış veya loop diüretik kullanımı eşlik etmesi; ayrıca sol ventrikül duvar kalınlığının ≥12 mm olması genel kriterlerdir.10–12 Ancak bu kriterler esnek biçimde uygulanmalıdır; çünkü: daha erken tanı konulması hastaneye yatışı azaltabilir. Sodyum-glukoz kotransporter-2 (SGLT2) inhibitörleri ve mineralokortikoid reseptör antagonistleri (MRA) ile kalp yetersizliği tedavisindeki gelişmeler, loop diüretik gereksinimi olmaksızın volüm durumunun kontrol edilmesini sağlayabilir. Bu nedenle kalp yetersizliği nedeniyle hastaneye yatış olmaması veya loop diüretik gereksiniminin bulunmaması, ATTR-CM hastalık modifiye edici tedavinin başlanmasına engel olmamalıdır. Ayrıca bazı ATTR-CM hastalarında (özellikle kadınlarda)59 sol ventrikül duvar kalınlığı ≥12 mm olmayabilir; dolayısıyla bu spesifik kriterin bulunmaması da tedavi başlanmasını engellememelidir. Öte yandan hastalık modifiye edici tedavinin olası yararı hakkında veri bulunmayan bazı hasta grupları vardır. Örneğin, ATTRv-CM’li bireylerin aile üyelerinde yapılan kademeli tarama sonucunda patojenik TTR varyantı taşıyan asemptomatik bireyler ve karpal tünel sendromu veya spinal stenozu olan bazı bireylerde bağ dokusu yapılarında transtiretin amiloid birikimi bulunmasına rağmen kardiyak hastalık kanıtının olmaması durumlarında tedavi fayda sağlamamıştır. Bu bireylerde daha sonra ATTR-CM gelişme olasılığı daha yüksek olsa da,3,4,19,22 mevcut kanıtlar tedavinin başlatılmasını desteklememektedir. Bununla birlikte ACT-EARLY (Acoramidis Transthyretin Amyloidosis Prevention Trial in the Young Study in Asymptomatic Carriers of a Pathogenic TTR Variant; NCT06563895) çalışması, transtiretin stabilizatörü acoramidisin kardiyomiyopati ve polinöropati gelişimi üzerindeki etkisini değerlendirecektir. Ayrıca nonsteroid antiinflamatuvar bir ilaç olan diflunisal transtiretin tetramerini stabilize ederek ATTRv polinöropatisinin ilerlemesini yavaşlatabilir,60,61 ve profilaktik kullanımı daha fazla araştırma konusudur. Bazı hastalarda hastalık çok ileri evrede olabilir ve bu nedenle hastalık modifiye edici tedaviden fayda sağlanamayabilir. İlacın onaylanmasına yol açan üç çalışmanın tümü ileri semptomları olan bireyleri dışlamıştır. Özellikle dışlama kriterleri şunlardır: belirgin fonksiyonel kısıtlılık (ATTR-ACT için 6 dakikalık yürüme mesafesi <100 m; ATTRibute-CM ve HELIOS-B için <150 m), yüksek natriüretik peptid düzeyleri (ATTRibute-CM ve HELIOS-B için N-terminal pro-B-tipi natriüretik peptid >8.500 pg/mL) ve ağır böbrek yetmezliği (ATTRibute-CM’de tahmini glomerüler filtrasyon hızı [eGFR] <15 mL/dk/1.73 m²; ATTR-ACT’te eGFR <25 mL/dk/1.73 m²; HELIOS-B’de eGFR <30 mL/dk/1.73 m²).0–12 İleri evre ATTR-CM olan bireylerde tedavi zararlı olmayabilir; ancak fayda gösterilmemiştir. Bu tür hastalarda, eşlik eden hastalıklara göre uygun ise kalp transplantasyonu değerlendirmesi için sevk edilmesi veya uygun değilse palyatif bakım konsültasyonu yapılması uygun olacaktır.62
4.2.2.2. Stabilizatör ile Susturucu Hastalık-Değiştirici Tedavi Arasında Seçim
Tafamidis, acoramidis ve vutrisiranın üç dönüm noktası niteliğindeki çalışmasının da plasebo kontrollü olması nedeniyle, herhangi bir ajanın diğerine göre göreceli üstünlüğünü değerlendirmeye olanak sağlayan doğrudan randomize klinik çalışma veya karşılaştırmalı etkinlik kanıtı bulunmamaktadır. Tümünün yan etki profili minimal olduğundan, bu durum da tedavi seçimini etkileyecek bir unsur değildir. Ayrıca bireysel klinik çalışmaların karşılaştırılması, çalışma popülasyonlarındaki farklılıklar nedeniyle sınırlıdır; daha güncel çalışmalar, daha düşük N-terminal pro–B-tipi natriüretik peptid düzeyleri, daha yüksek 6 dakikalık yürüme mesafesi, daha iyi yaşam kalitesi ve her bir çalışmanın plasebo kollarında bile giderek daha düşük olay oranları ile gösterildiği üzere, hastalığın daha erken evrelerindeki bireyleri içermektedir (Tablo 2). Ayrıca stabilizatör tedavisi sonrasında serum transtiretin düzeylerindeki farklı değişimlerin klinik üstünlüğü gösterdiğine dair bugüne kadar herhangi bir kanıt bulunmamaktadır. Bu nedenle aktif kontrollü klinik çalışmalar olmadan, ATTR-CM’li bireylerde başlangıç tedavisi olarak tafamidis, acoramidis veya vutrisirandan hangisinin üstün olduğu bilinmemektedir.
Dolayısıyla mevcut verilere dayanarak tedavi seçimi şu faktörlere göre yapılmalıdır:
- maliyet,
- geri ödeme kuruluşlarının tercihleri doğrultusunda erişim,
- uygulama yolu ve sıklığı konusunda bireysel tercih (günde bir kez oral, günde iki kez oral veya A vitamini desteği ile birlikte her 3 ayda bir subkutan enjeksiyon).
Önemli bir istisna, ATTRv-CM ve amiloid polinöropatisi olan bireylerdir. Bu kişilerde transtiretin susturucu tedavi olan vutrisiran tercih edilebilir; çünkü klinik çalışmalar transtiretin susturucularının ATTRv-polinöropatide fayda sağladığını göstermektedir.⁶³⁻⁶⁵ Ayrıca, ATTRv-CM’li bireylerde görülen polinöropatinin, daha sık görülen kas-iskelet sistemi bulgularına (örneğin karpal tünel sendromu, spinal stenoz) kıyasla daha nadir olduğu da belirtilmelidir.²⁵ ²⁶ Transtiretin susturucu tedavi ATTRv-polinöropatide etkili olmakla birlikte, bu tedavinin kas-iskelet sistemi bulgularını azalttığını gösteren veri bulunmamaktadır. Bu nedenle transtiretin susturucu tedavi bu durumları spesifik olarak tedavi etmek amacıyla endike değildir.
4.2.2.3. Kombine Stabilizatör ve Susturucu Tedavinin Rolü
ATTR-CM’de kombinasyon tedavisinin gerekçesi, etkinliği artırma ve hastalık progresyonu riskini azaltma potansiyeline dayanır; ancak bunun karşılığında maliyet artışı söz konusudur (jenerik seçeneklerin kullanıma girmesiyle finansal etkinin azalması beklenebilir). Bugüne kadar, transtiretin düzeylerinde belirgin azalma sağlandıktan sonra dolaşımda kalan transtiretinin stabilize edilmesinin ek bir fayda sağlayıp sağlamadığı bilinmemektedir. Mevcut klinik çalışma verileri, iki stabilizatörün birlikte kullanımı ya da bir stabilizatör ile bir susturucunun kombinasyon halinde kullanımını desteklememektedir.
HELIOS-B çalışmasında katılımcıların %40’ı başlangıçta tafamidis kullanmaktaydı. Kalan %60’lık hasta grubu monoterapi grubunu oluşturmakta olup, bu grubun yaklaşık %20’sinde randomizasyondan sonra ortalama yaklaşık 17 ay içinde tafamidis tedavisi başlatılmıştır. HELIOS-B çalışması özellikle vutrisiran ve tafamidis kombinasyon tedavisinin etkinliğini değerlendirmek üzere yeterli güçte tasarlanmamış olsa da, başlangıçta tafamidis tedavisine vutrisiran eklenmesi bu alt grupta klinik sonlanım noktalarında istatistiksel olarak anlamlı bir iyileşme sağlamamıştır. ⁶⁶⁻⁶⁸ Bu nedenle mevcut kanıtlara dayanarak transtiretin susturucu ve stabilizatör kombinasyon tedavisinin rutin kullanımı önerilmemektedir.
Devam etmekte olan CARDIO-TTRansform (Transtiretin Aracılı Amiloid Kardiyomiyopatili Katılımcılarda Eplontersen’in Etkinlik ve Güvenliliğinin Değerlendirilmesi Çalışması; NCT0413617) çalışması bu konuyu aydınlatabilir. CARDIO-TTRansform çalışmasına 1.432 katılımcı dahil edilmiş olup bunların %70’i eş zamanlı tafamidis tedavisi almaktadır. ⁶⁹ Sonuçların 2026 yılında açıklanması beklenmektedir. Stabilizatör tedavisi ile eş zamanlı tedavi alan katılımcı sayısının yüksek olması nedeniyle bu çalışma, bu popülasyonda kombinasyon tedavisine ilişkin kritik bilgiler sağlayabilir; ancak kombinasyon tedavisi ile tekli tedavi arasındaki farkı saptama gücü yine de sınırlı kalabilir.
4.2.2.4. Hastalık Progresyonu ve Tedavi Ayarlamalarının Rolü
Günümüzde hastalık-değiştirici tedaviye yanıtın veya tedavi başarısızlığının neyi ifade ettiğine dair yaygın olarak kabul edilmiş bir tanım bulunmamaktadır. ATTR-CM’li birçok bireyde kalp yetersizliği semptomlarında kötüleşme, yeni aritmilerin gelişmesi veya her ikisi görülebilmekle birlikte, bunun başlangıçtaki hastalığın sekellerini mi yoksa devam eden ATTR fibril birikimini mi yansıttığı net değildir. ⁷⁰
Etkilenen popülasyonun ileri yaşı (ATTR-CM klinik çalışmalarında medyan yaş 75–77 yıl) ¹⁰⁻¹² ve eşlik eden hastalıklar (örneğin böbrek fonksiyon bozukluğu, frailty) hastalık progresyonunu, transtiretin yanlış katlanması ve agregasyonu ile ilişkili mekanizmalardan daha fazla açıklıyor olabilir. Mevcut durumda kötüleşen semptomlar karşısında hastalık-değiştirici tedavinin ayarlanmasına rehberlik edecek yeterli kanıt bulunmamaktadır.
4.2.3. Kalp Yetersizliği Yönetimi
4.2.3.1. Restriktif Fizyolojinin Etkileri
Restriktif fizyolojiye sahip bireylerde basınç-hacim ilişkilerinde fizyolojik değişiklikler görülür. Ventriküler kompliyansın bozulması sol ve sağ dolum basınçlarının artmasına yol açar; azalmış ve nispeten sabit bir strok volüm nedeniyle kalp debisinin sürdürülebilmesi için kalp hızına bağımlılık gelişir; ayrıca artmış ventrikül sertliği ve anormal arteriyel elastans nedeniyle vasküler-ventriküler eşleşme bozulur.⁴¹ ⁷¹ Bu hemodinamik değişiklikler preload bağımlılığı ve afterload intoleransı ile sonuçlanır ve kalp yetersizliği yönetiminde bireye özgü bir yaklaşım gerektirir (Şekil 3, Tablo 3).
4.2.3.2. Diüretikler
Loop diüretikler pulmoner ve sistemik konjesyonu azaltır; ancak preload bağımlılığı ve aşırı diürez sonucu hipotansiyon, azalmış strok volüm ve akut böbrek hasarı riski nedeniyle dikkatli şekilde titre edilmelidir. Diüretik direnci gelişen bireylerde furosemidden daha yüksek biyoyararlanıma sahip torsemid veya bumetanide geçilmesi ya da tiyazidlerin eklenmesiyle (örneğin metolazon) ardışık nefron blokajı uygulanması düşünülebilir; bu yaklaşım elektrolitlerin dikkatli izlenmesini gerektirir. Yüksek başlangıç diüretik gereksinimi⁷² ve diüretik tedavisinin yoğunlaştırılması gereksinimi⁶⁷ ⁷³ daha kötü prognoz ile ilişkilidir.
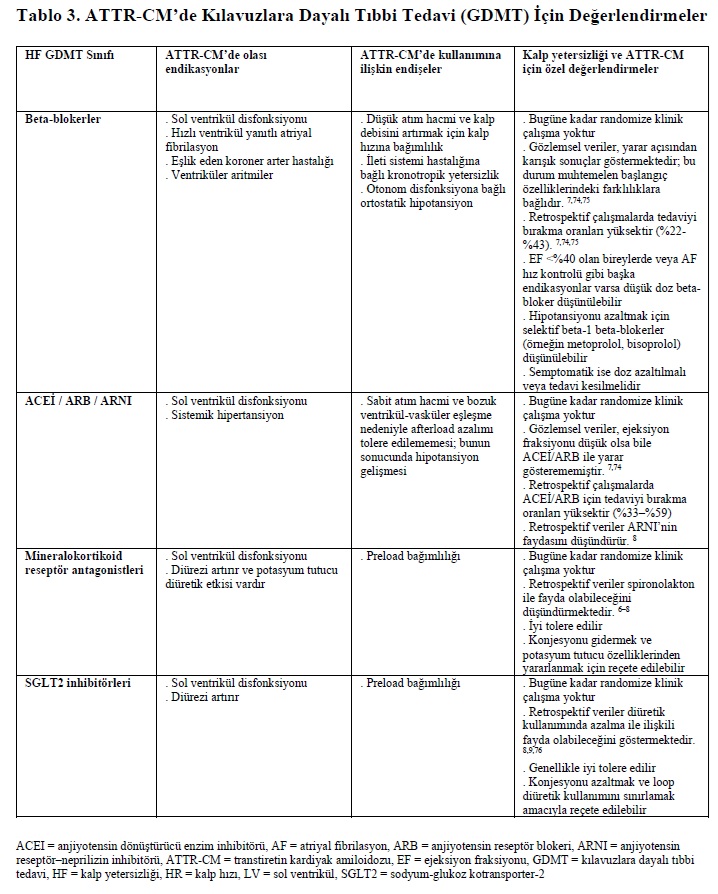
4.2.3.3. Geleneksel Kılavuz Yönlendirmeli Tıbbi Tedavinin Endikasyonları ve Dezavantajları
Tarihsel olarak ATTR-CM’li bireylerde beta-bloker kullanımı konusunda endişe vardır. Bunun nedeni, kalp debisini sürdürebilmek için kalp hızına bağımlılık, iletim sisteminin amiloid infiltrasyonu sonucu kronotropik yetersizlik ve otonom disfonksiyondur. Gözlemsel veriler heterojendir ve çalışmalarda beta-bloker tedavisinin kesilme oranları %22 ile %43 arasında değişmektedir.⁷ ⁷⁴ ⁷⁵ Fayda göstermeyen bir çalışmada daha ileri evre hastalar yer almakta ve daha yüksek dozlarda nonselektif beta-blokerler kullanılmaktaydı.⁷⁴ Buna karşılık en büyük kohort çalışması, düşük doz beta-blokerlerin (bisoprolol ≤2.5 mg/gün) ejeksiyon fraksiyonu ≤%40 olan bireylerde faydalı olabileceğini göstermiştir.⁷ Bu nedenle özellikle atriyal fibrilasyonda hız kontrolü gerekiyorsa, ejeksiyon fraksiyonu ≤%40 olan bireylerde düşük doz beta-blokerler dikkatle düşünülebilir; intolerans gelişmesi durumunda doz azaltımı veya tedavinin kesilmesi için düşük bir eşik benimsenmelidir.
Retrospektif gözlemsel çalışmalar, ejeksiyon fraksiyonu düşük olup olmamasına bakılmaksızın vazodilatör etkili anjiyotensin dönüştürücü enzim inhibitörleri veya anjiyotensin reseptör blokerleri ile klinik fayda gösterememiştir ve yan etkiler nedeniyle tedavi kesilme oranları %33–59 arasında yüksektir.⁷ Buna karşın PARADIGM-HF çalışmasının (Prospective Comparison of ARNI [Angiotensin Receptor–Neprilysin Inhibitor] With ACEI [Angiotensin Converting–Enzyme Inhibitor] to Determine Impact on Global Mortality and Morbidity in Heart Failure) post-hoc analizinde, ATTR-CM klinik skoru ile amiloidoz olabileceği düşünülen HFmrEF ve HFpEF alt grubunda sakubitril/valsartan tedavisinin faydalı olduğu gösterilmiştir.³⁵ Vazodilatörler semptomatik ortostaz veya akut böbrek hasarı nedeniyle tolere edilemeyebilir; ancak bu verilere dayanarak anjiyotensin reseptör neprilizin inhibitörü dikkatle denenebilir.
Benzer şekilde, TOPCAT-Americas çalışmasının (Treatment of Preserved Cardiac Function Heart Failure With Aldosterone Antagonist in the Americas) HFmrEF ve HFpEF’li bireylerde spironolakton ile plasebonun karşılaştırıldığı ve amiloidoz açısından zenginleştirilmiş alt grup analizinde, genel popülasyona benzer tedavi faydası gösterilmiştir.³⁵ ⁸ Diğer retrospektif analizlerde de benzer bulgular gözlenmiş⁶ ve tedavi kesilme oranı yalnızca %8 olup kabul edilebilir tolerans bildirilmiştir.⁷ ATTR-CM’de eplerenon veya finerenon ile ilgili henüz kanıt bulunmamakla birlikte, mineralokortikoid reseptör antagonistlerinin faydasının muhtemelen sınıf etkisi olduğu düşünülebilir. Diüretik gereksinimi olan ATTR-CM’li bireylerde konjesyonu azaltmak amacıyla MRA’lar bir seçenek olabilir. SGLT2 inhibitörleri de ATTR-CM’li bireylerde klinik fayda sağlayabilir.⁹ ⁷⁶ DELIVER çalışmasının (Dapagliflozin Evaluation to Improve the Lives of Patients With Preserved Ejection Fraction Heart Failure) retrospektif analizinde, ATTR-CM fenotipi ile uyumlu HFmrEF ve HFpEF’li bireylerde dapagliflozinin fayda sağladığı gösterilmiştir.⁸ Çok merkezli bir kohort çalışmasında SGLT2 inhibitörlerinin tedavi kesilme oranı yalnızca %4.5 olup, fonksiyonel durumda iyileşme, kardiyak biyobelirteçlerde azalma, böbrek fonksiyonunda stabilizasyon ve tüm nedenlere bağlı ölüm ile kalp yetersizliği nedeniyle hastaneye yatışta azalma ile ilişkili bulunmuştur.⁹ Bu bulguları destekler şekilde tek merkezli bir kohort çalışmasında SGLT2 inhibitörü kullanımının daha fazla kilo kaybı ve daha düşük loop diüretik dozu ile ilişkili olduğu gösterilmiştir.⁷⁶ Tüm bu veriler birlikte değerlendirildiğinde, diüretik tedavisine ihtiyaç duyan ATTR-CM’li bireylerde hem MRA’ların hem de SGLT2 inhibitörlerinin konjesyonu azaltmada etkili seçenekler olabileceğini düşündürmektedir. Bununla birlikte MRA ve SGLT2 inhibitörlerinin ATTR-CM’li tüm bireylerde rutin kullanımı henüz kanıtlarla desteklenmemektedir.
4.3. Gelecekteki Tedaviler
4.3.1. Gen Düzenleme ile Transtiretin Susturma
Transtiretin haberci ribonükleik asidi (mRNA) susturucularının gösterilmiş etkinliği, genomik TTR’nin kalıcı olarak değiştirilmesinin de benzer şekilde etkili olabileceğini düşündürmektedir. CRISPR (Clustered Regularly Interspaced Short Palindromic Repeats)–Cas9 ajanı nexiguran ziclumeran (nex-z) ile yürütülen çalışmaya ilişkin ön veriler, 12 ayda transtiretin düzeylerinde kalıcı azalma ve kardiyak biyobelirteçler ile fonksiyonel kapasitede stabilizasyon göstermektedir.⁶⁹
Nex-z’nin başlıca avantajı tek doz uygulama olmasıdır; ayrıca vutrisiran (%81)⁷⁷ veya eplontersen (%82)¹² ile bildirilen oranlardan daha yüksek derecede transtiretin baskılanması (%89) sağlayabilme potansiyeline sahiptir. Nex-z için faz 3 bir çalışma devam etmektedir (MAGNITUDE [Transtiretin Amiloidozu ile Kardiyomiyopatili Katılımcılarda NTLA-2001’in Faz 3 Çalışması (ATTR-CM)] NCT06128629)⁷⁸ ve tahmini tamamlanma tarihi 2028’dir. Bununla birlikte, genomik TTR’nin kalıcı olarak değiştirilmesinin göreceli klinik faydası, güvenliği ve maliyeti ile halihazırda mevcut transtiretin mRNA susturucuları ile karşılaştırıldığında üstünlüğü henüz net değildir.
4.3.2. Monoklonal Antikorlarla Transtiretin Depo Azaltıcı Tedaviler
Mevcut hastalık-değiştirici tedaviler transtiretin amiloid fibrillerinin birikimini yavaşlatmak veya durdurmakta ve ATTR-CM progresyonunu yavaşlatmaktadır; ancak hastalığı geri döndüremezler. Buna karşılık transtiretin amiloid birikimlerinin ortadan kaldırılması miyokardiyal kompliyansı yeniden sağlayabilir, hasarı tersine çevirebilir ve klinik sonuçları iyileştirebilir.⁷⁹
Yanlış katlanmış transtiretini tanıyan ve makrofaj aracılı temizlenme mekanizmalarını aktive ederek yıkımı kolaylaştıran hedefe yönelik monoklonal antikorların geliştirilmesi, ATTR fibril azaltıcı ajanların terapötik potansiyelini temsil etmektedir.⁸⁰ ⁸¹ Bu ajanlardan biri faz 3 klinik çalışma için hasta alımını tamamlamıştır (ALXN2220, önceki adıyla NI006; DepleTTR-CM [ATTR-CM’li Erişkinlerde ALXN2220’nin Plasebo ile Karşılaştırıldığı Çalışma]; NCT06183931)⁸² ve tahmini tamamlanma tarihi 2027’dir. Bir diğer ajan ise faz 2 aşamasındadır (coramitug, önceki adıyla PRX-0004; NCT05442047)⁸³ ve hasta alımı Mayıs 2025’te tamamlanmıştır; bunu takiben bir faz 3 çalışmasının yapılması beklenmektedir.
Bu ajanlar güvenlik açısından sorun oluşturmadan etkili oldukları doğrulanırsa, hastalığın ileri evrelerinde belirgin semptom yükü ve organ tutulumu olan bireylerde ATTR-CM’nin “ters yeniden şekillenmesine” (reverse remodeling) yol açabilecek önemli bir terapötik ilerleme sağlayabilir.
4.4. Sonuçlar
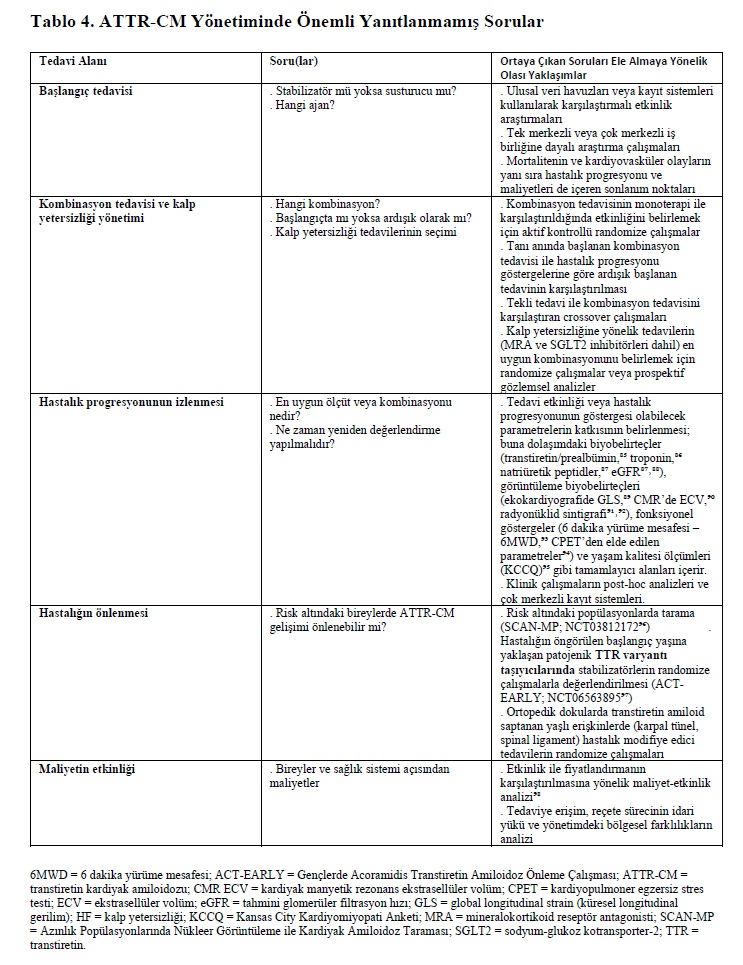
Son on yılda ATTR-CM’nin erken tanınması, doğru tanısı ve etkili tedavisindeki paralel ilerlemelerin önemli sonucu, amiloid tedavilerine yönelik dönüm noktası çalışmalarında giderek daha sağlıklı hasta popülasyonlarının yer almasıdır. Özellikle en güncel çalışma olan HELIOS-B’nin tedavi kolunda tüm nedenlere bağlı ölüm oranı, yaşa göre beklenen 3 yıllık mortalite oranına yaklaşmıştır.⁸⁴ Bununla birlikte bu önemli ilerlemelere rağmen birçok önemli soru hâlâ yanıtlanmamıştır (Tablo 4).⁶⁹ Günümüzde onaylanmış transtiretin hastalık-değiştirici tedaviler arasında iki transtiretin stabilizatörü (acoramidis ve tafamidis) ve bir transtiretin susturucu (vutrisiran) bulunmaktadır. Böylece klinisyenlerin artık ATTR-CM ile yaşayan bireylerde yaşam kalitesini korumak ve sağkalımı artırmak için birden fazla tedavi seçeneği vardır. Şu anda hiçbir çalışma bir ajanın diğerine üstün olduğunu göstermemiştir; ayrıca rutin kombinasyon tedavisini önermek veya hastalık progresyonunu azaltmak amacıyla tedaviyi değiştirmek için yeterli veri bulunmamaktadır. Bununla birlikte devam eden çalışmalar, bazı yanıtlanmamış soruların açıklığa kavuşmasına ve ATTR-CM’li bireyler için en uygun bakımın geliştirilmesine katkı sağlayabilir.
Referanslar;
- Gonzalez-Lopez E, Gallego-Delgado M, Guzzo-Merello G, et al. Wild-type transthyretin amyloidosis as a cause of heart failure with preserved ejection fraction. Eur Heart J. 2015;36:2585–2594.
- Castano A, Narotsky DL, Hamid N, et al. Unveiling transthyretin cardiac amyloidosis and its predictors among elderly patients with severe aortic stenosis undergoing transcatheter aortic valve replacement. Eur Heart J. 2017;38:2879–2887.
- Sperry BW, Reyes BA, Ikram A, et al. Tenosynovial and cardiac amyloidosis in patients undergoing carpal tunnel release. J Am Coll Cardiol. 2018;72:2040–2050.
- Westermark P, Westermark GT, Suhr OB, et al. Transthyretin-derived amyloidosis: probably a common cause of lumbar spinal stenosis. Ups J Med Sci. 2014;119:223–228.
- Gillmore JD, Maurer MS, Falk RH, et al. Nonbiopsy diagnosis of cardiac transthyretin amyloidosis. Circulation. 2016;133:2404–2412.
- Sperry BW, Hanna M, Shah SJ, et al. Spironolactone in patients with an echocardiographic HFpEF phenotype suggestive of cardiac amyloidosis: results from TOPCAT. JACC Heart Fail. 2021;9:795–802.
- Ioannou A, Massa P, Patel RK, et al. Conventional heart failure therapy in cardiac ATTR amyloidosis. Eur Heart J. 2023;44:2893–2907.
- Inciardi RM, Vaduganathan M, Claggett B, et al. Application of a transthyretin amyloid cardiomyopathy score to heart failure with mildly reduced or preserved ejection fraction. Eur J Heart Fail. 2025;12:3012–3016.
- Porcari A, Cappelli F, Nitsche C, et al. SGLT2 inhibitor therapy in patients with transthyretin amyloid cardiomyopathy. J Am Coll Cardiol. 2024;83:2411–2422.
- Maurer MS, Schwartz JH, Gundapaneni B, et al. Tafamidis treatment for patients with transthyretin amyloid cardiomyopathy. N Engl J Med. 2018;379:1007–1016.
- Gillmore JD, Judge DP, Cappelli F, et al. Efficacy and safety of acoramidis in transthyretin amyloid cardiomyopathy. N Engl J Med. 2024;390:132–142.
- Fontana M, Berk JL, Gillmore JD, et al. Vutrisiran in patients with transthyretin amyloidosis with cardiomyopathy. N Engl J Med. 2025;392:33–44.
- Heidenreich PA, Bozkurt B, Aguilar D, et al. 2022 AHA/ACC/HFSA guideline for the management of heart failure: a report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. J Am Coll Cardiol. 2022;79:e263–e421.
- Hicks KA, Tcheng JE, Bozkurt B, et al. 2014 ACC/AHA key data elements and definitions for cardiovascular endpoint events in clinical trials: a report of the American College of Cardiology/American Heart Association Task Force on Clinical Data Standards (Writing Committee to Develop Cardiovascular Endpoints Data Standards). J Am Coll Cardiol. 2015;66:403–469.
- Muchtar E, Gertz MA, Kyle RA, et al. A modern primer on light chain amyloidosis in 592 patients with mass spectrometry-verified typing. Mayo Clin Proc. 2019;94:472–483.
- Mohammed SF, Mirzoyev SA, Edwards WD, et al. Left ventricular amyloid deposition in patients with heart failure and preserved ejection fraction. JACC Heart Fail. 2014;2:113–122.
- Hahn VS, Yanek LR, Vaishnav J, et al. Endomyocardial biopsy characterization of heart failure with preserved ejection fraction and prevalence of cardiac amyloidosis. JACC Heart Fail. 2020;8:712–724.
- Basdavanos A, Maurer MS, Ives L, et al. Prevalence of orthopedic manifestations in patients with cardiac amyloidosis with a focus on shoulder pathologies. Am J Cardiol. 2023;190:67–74.
- Yanagisawa A, Ueda M, Sueyoshi T, et al. Amyloid deposits derived from transthyretin in the ligamentum flavum as related to lumbar spinal canal stenosis. Mod Pathol. 2015;28:201–207.
- Moore ZJ, Rizkalla JM, Weiner J, et al. Transthyretin amyloidosis in spinal canal stenosis: a systematic review. J Orthop. 2024;53:133–139.
- Geller HI, Singh A, Alexander KM, et al. Association between ruptured distal biceps tendon and wild-type transthyretin cardiac amyloidosis. JAMA. 2017;318:962–963.
- Nakagawa M, Sekijima Y, Yazaki M, et al. Carpal tunnel syndrome: a common initial symptom of systemic wild-type ATTR (ATTRwt) amyloidosis. Amyloid. 2016;23:58–63.
- Connors LH, Sam F, Skinner M, et al. Heart failure resulting from age-related cardiac amyloid disease associated with wild-type transthyretin: a prospective, observational cohort study. Circulation. 2016;133:282–290.
- Kleefeld F, Scherret E, Knebel F, et al. Same same, but different? The neurological presentation of wild-type transthyretin (ATTRwt) amyloidosis. Amyloid. 2022;29:92–101.
- Wajnsztajn Yungher F, Kim A, Boehme A, et al. Peripheral neuropathy symptoms in wild-type transthyretin amyloidosis. J Peripher Nerv Syst. 2020;25:265–272.
- Russell A, Hahn C, Chhibber S, et al. Utility of neuropathy screening for wild-type transthyretin amyloidosis patients. Can J Neurol Sci. 2021;48:607–615.
- Quarta CC, Solomon SD, Uraizee I, et al. Left ventricular structure and function in transthyretin-related versus light-chain cardiac amyloidosis. Circulation. 2014;129:1840–1849.
- Jiang Z, Zhuang S, Tang M, et al. Diagnostic value of the voltage-to-mass ratio in biopsy-proven cardiac amyloidosis. Ann Noninvasive Electrocardiol. 2024;29:e70026.
- Dorbala S, Ando Y, Bokhari S, et al. ASNC/AHA/ASE/EANM/HFSA/ISA/SCMR/SNMMI expert consensus recommendations for multimodality imaging in cardiac amyloidosis: part 1 of 2—evidence base and standardized methods of imaging. J Nucl Cardiol. 2019;26:2065–2123.
- Cuddy SAM, Chetrit M, Jankowski M, et al. Practical points for echocardiography in cardiac amyloidosis. J Am Soc Echocardiogr. 2022;35:A31–A40.
- Pagourelias ED, Mirea O, Duchenne J, et al. Echo parameters for differential diagnosis in cardiac amyloidosis: a head-to-head comparison of deformation and nondeformation parameters. Circ Cardiovasc Imaging. 2017;10:e005588.
- Martinez-Naharro A, Treibel TA, Abdel-Gadir A, et al. Magnetic resonance in transthyretin cardiac amyloidosis. J Am Coll Cardiol. 2017;70:466–477.
- Vergaro G, Castiglione V, Aimo A, et al. N-terminal pro-B-type natriuretic peptide and high-sensitivity troponin T hold diagnostic value in cardiac amyloidosis. Eur J Heart Fail. 2023;25:335–346.
- De Michieli L, AbouEzzeddine OF, Abbasi MA, et al. Biomarkers to predict abnormal technetium-99m pyrophosphate scans in patients with suspected transthyretin amyloidosis. JACC CardioOncol. 2025;7:70–78.
- Davies DR, Redfield MM, Scott CG, et al. A simple score to identify increased risk of transthyretin amyloid cardiomyopathy in heart failure with preserved ejection fraction. JAMA Cardiol. 2022;7:1036–1044.
- Grogan M, Lopez-Jimenez F, Cohen-Shelly M, et al. Artificial intelligence-enhanced electrocardiogram for the early detection of cardiac amyloidosis. Mayo Clin Proc. 2021;96:2768–2778.
- Slivnick JA, Hawkes W, Oliveira J, et al. Cardiac amyloidosis detection from a single echocardiographic video clip: a novel artificial intelligence-based screening tool. Eur Heart J. 2025;46(40):4090–4101.
- Weberling LD, Ochs A, Benovoy M, et al. Machine learning to automatically differentiate hypertrophic cardiomyopathy, cardiac light chain, and cardiac transthyretin amyloidosis: a multicenter CMR study. Circ Cardiovasc Imaging. 2025;18:e017761.
- Katzmann JA, Abraham RS, Dispenzieri A, et al. Diagnostic performance of quantitative kappa and lambda free light chain assays in clinical practice. Clin Chem. 2005;51:878–881.
- Long TE, Indridason OS, Palsson R, et al. Defining new reference intervals for serum free light chains in individuals with chronic kidney disease: results of the iStopMM study. Blood Cancer J. 2022;12:133.
- Kittleson MM, Ruberg FL, Ambardekar AV, et al. 2023 ACC expert consensus decision pathway on comprehensive multidisciplinary care for the patient with cardiac amyloidosis: a report of the American College of Cardiology Solution Set Oversight Committee. J Am Coll Cardiol. 2023;81:1076–1126.
- Cohen OC, Sharpley F, Gilbertson JA, et al. The value of screening biopsies in light-chain (AL) and transthyretin (ATTR) amyloidosis. Eur J Haematol. 2020;105:352–356.
- Quarta CC, Gonzalez-Lopez E, Gilbertson JA, et al. Diagnostic sensitivity of abdominal fat aspiration in cardiac amyloidosis. Eur Heart J. 2017;38:1905–1908.
- Fine NM, Arruda-Olson AM, Dispenzieri A, et al. Yield of noncardiac biopsy for the diagnosis of transthyretin cardiac amyloidosis. Am J Cardiol. 2014;113:1723–1727.
- Gertz MA, Dispenzieri A. Systemic amyloidosis recognition, prognosis, and therapy: a systematic review. JAMA. 2020;324:79–89.
- Kyle RA, Gertz MA. Primary systemic amyloidosis: clinical and laboratory features in 474 cases. Semin Hematol. 1995;32:45–59.
- Hansen CT, Møller HEH, Rojek AM, et al. Combined subcutaneous fat aspirate and skin tru-cut biopsy for amyloid screening in patients with suspected systemic amyloidosis. Molecules. 2021;26(12):3649.
- van Gameren I, Hazenberg BP, Bijzet J, et al. Diagnostic accuracy of subcutaneous abdominal fat tissue aspiration for detecting systemic amyloidosis and its utility in clinical practice. Arthritis Rheum. 2006;54:2015–2021.
- Hutchison CA, Harding S, Hewins P, et al. Quantitative assessment of serum and urinary polyclonal free light chains in patients with chronic kidney disease. Clin J Am Soc Nephrol. 2008;3:1684–1690.
- Miller EJ, Campisi R, Shah NR, et al. Radiopharmaceutical supply disruptions and the use of (99m)Tc-hydroxymethylene diphosphonate as an alternative to (99m)Tc-pyrophosphate for the diagnosis of transthyretin cardiac amyloidosis: an ASNC information statement. J Nucl Cardiol. 2022;29:2748–2760.
- Khor YM, Cuddy SAM, Singh V, et al. (99m)Tc bone-avid tracer cardiac scintigraphy: role in noninvasive diagnosis of transthyretin cardiac amyloidosis. Radiology. 2023;306:e221082.
- Damy T, Garcia-Pavia P, Hanna M, et al. Efficacy and safety of tafamidis doses in the Tafamidis in Transthyretin Cardiomyopathy Clinical Trial (ATTR-ACT) and long-term extension study. Eur J Heart Fail. 2021;23:277–285.
- Lockwood PA, Le VH, O’Gorman MT, et al. The bioequivalence of tafamidis 61-mg free acid capsules and tafamidis meglumine 4 × 20-mg capsules in healthy volunteers. Clin Pharmacol Drug Dev. 2020;9:849–854.
- Lee A. Acoramidis: first approval. Drugs. 2025;85:833–837.
- Judge DP, Alexander KM, Cappelli F, et al. Efficacy of acoramidis on all-cause mortality and cardiovascular hospitalization in transthyretin amyloid cardiomyopathy. J Am Coll Cardiol. 2025;85:1003–1014.
- Judge DP, Gillmore JD, Alexander KM, et al. Long-term efficacy and safety of acoramidis in ATTR-CM: initial report from the open-label extension of the ATTRibute-CM trial. Circulation. 2025;151:601–611.
- Brannagan TH 3rd, Berk JL, Gillmore JD, et al. Liver-directed drugs for transthyretin-mediated amyloidosis. J Peripher Nerv Syst. 2022;27:228–237.
- Merative. Micromedex RED BOOK. Accessed July 2025. https://www.merative.com/documents/micromedex-red-book
- Bruno M, Castano A, Burton A, et al. Transthyretin amyloid cardiomyopathy in women: frequency, characteristics, and diagnostic challenges. Heart Fail Rev. 2021;26:35–45.
- Tojo K, Sekijima Y, Kelly JW, et al. Diflunisal stabilizes familial amyloid polyneuropathy-associated transthyretin variant tetramers in serum against dissociation required for amyloidogenesis. Neurosci Res. 2006;56:441–449.
- Berk JL, Suhr OB, Obici L, et al. Repurposing diflunisal for familial amyloid polyneuropathy: a randomized clinical trial. JAMA. 2013;310:2658–2667.
- Ambardekar AV, Fontana M, Maurer MS, et al. How to identify cardiac amyloidosis patients who might benefit from cardiac transplantation. JACC Heart Fail. 2023;11:115–120.
- Adams D, Gonzalez-Duarte A, O’Riordan WD, et al. Patisiran, an RNAi therapeutic, for hereditary transthyretin amyloidosis. N Engl J Med. 2018;379:11–21.
- Benson MD, Waddington-Cruz M, Berk JL, et al. Inotersen treatment for patients with hereditary transthyretin amyloidosis. N Engl J Med. 2018;379:22–31.
- Adams D, Tournev IL, Taylor MS, et al. Efficacy and safety of vutrisiran for patients with hereditary transthyretin-mediated amyloidosis with polyneuropathy: a randomized clinical trial. Amyloid. 2023;30:1–9.
- Witteles RM, Garcia-Pavia P, Damy T, et al. Vutrisiran improves survival and reduces cardiovascular events in ATTR amyloid cardiomyopathy: HELIOS-B. J Am Coll Cardiol. 2025;85:1959–1970.
- Fontana M, Maurer MS, Gillmore JD, et al. Outpatient worsening heart failure in patients with transthyretin amyloidosis with cardiomyopathy in the HELIOS-B trial. J Am Coll Cardiol. 2025;85:753–761.
- Sheikh FH, Habib G, Tang WHW, et al. Impact of vutrisiran on functional capacity and quality of life in transthyretin amyloidosis with cardiomyopathy. J Am Coll Cardiol. 2025;85:1943–1955.
- Griffin JM, Grodin JL, Ruberg FL, et al. Current landscape of therapies for transthyretin amyloid cardiomyopathy. JACC Heart Fail. 2025;13:685–694.
- Maurer MS. A question in the era of multiple effective therapies for transthyretin amyloid cardiomyopathy (ATTR-CM): is transthyretin biology a driver of disease progression? J Card Fail. 2025;31:746–747.
- Bhuiyan T, Helmke S, Patel AR, et al. Pressure-volume relationships in patients with transthyretin (ATTR) cardiac amyloidosis secondary to V122I mutations and wild-type transthyretin: Transthyretin Cardiac Amyloid Study (TRACS). Circ Heart Fail. 2011;4:121–128.
- Cheng RK, Levy WC, Vasbinder A, et al. Diuretic dose and NYHA functional class are independent predictors of mortality in patients with transthyretin cardiac amyloidosis. JACC CardioOncol. 2020;2:414–424.
- Ioannou A, Cappelli F, Emdin M, et al. Stratifying disease progression in patients with cardiac ATTR amyloidosis. J Am Coll Cardiol. 2024;83:1276–1291.
- Cheng RK, Vasbinder A, Levy WC, et al. Lack of association between neurohormonal blockade and survival in transthyretin cardiac amyloidosis. J Am Heart Assoc. 2021;10:e022859.
- Barge-Caballero G, Barge-Caballero E, Lopez-Perez M, et al. Beta-blocker exposure and survival in patients with transthyretin amyloid cardiomyopathy. Mayo Clin Proc. 2022;97:261–273.
- Lang FM, Teruya S, Weinsaft A, et al. Sodium-glucose cotransporter 2 inhibitors for transthyretin amyloid cardiomyopathy: analyses of short-term efficacy and safety. Eur J Heart Fail. 2024;26:938–947.
- Fontana M, Solomon SD, Kachadourian J, et al. CRISPR-Cas9 gene editing with nexiguran ziclumeran for ATTR cardiomyopathy. N Engl J Med. 2024;391:2231–2241.
- MAGNITUDE. A Phase 3 Study of NTLA-2001 in Participants With Transthyretin Amyloidosis With Cardiomyopathy (ATTR-CM). ClinicalTrials.gov. Identifier: NCT06128629. Accessed June 2025. https://clinicaltrials.gov/study/NCT06128629
- Fontana M, Gilbertson J, Verona G, et al. Antibody-associated reversal of ATTR amyloidosis-related cardiomyopathy. N Engl J Med. 2023;388:2199–2201.
- Garcia-Pavia P, Mercuri MF, Kahr PC. Antibody NI006 for cardiac transthyretin amyloid depletion. Reply. N Engl J Med. 2023;389:1249.
- Suhr OB, Grogan M, Silva AMD, et al. PRX004 in variant amyloid transthyretin (ATTRv) amyloidosis: results of a phase 1, open-label, dose-escalation study. Amyloid. 2025;32:14–21.
- Study of ALXN2220 Versus Placebo in Adults With ATTR-CM (DepleTTR-CM). ClinicalTrials.gov. Identifier: NCT06183931. Accessed June 2025. https://clinicaltrials.gov/study/NCT06183931
- A Research Study to Look at How a New Medicine Called NNC6019-0001 Works and How Safe It Is for People Who Have Heart Disease Due to Transthyretin (TTR) Amyloidosis. ClinicalTrials.gov. Identifier: NCT05442047. Accessed June 2025. https://clinicaltrials.gov/study/NCT05442047
- Girard AA, Sperry BW. Contextualizing the results of HELIOS-B in the broader landscape of clinical trials for the treatment of transthyretin cardiac amyloidosis. Heart Fail Rev. 2025;30:69–73.
- Maurer MS, Judge DP, Gillmore JD, et al. Early increase in serum transthyretin by acoramidis independently predicts improved survival in TTR amyloid cardiomyopathy. J Am Coll Cardiol. 2025;85:1911–1923.
- Grogan M, Scott CG, Kyle RA, et al. Natural history of wild-type transthyretin cardiac amyloidosis and risk stratification using a novel staging system. J Am Coll Cardiol. 2016;68:1014–1020.
- Gillmore JD, Damy T, Fontana M, et al. A new staging system for cardiac transthyretin amyloidosis. Eur Heart J. 2018;39:2799–2806.
- Law S, Petrie A, Chacko L, et al. Disease progression in cardiac transthyretin amyloidosis is indicated by serial calculation of National Amyloidosis Centre transthyretin amyloidosis stage. ESC Heart Fail. 2020;7:3942–3949.
- Huntjens PR, Zhang KW, Soyama Y, et al. Prognostic utility of echocardiographic atrial and ventricular strain imaging in patients with cardiac amyloidosis. JACC Cardiovasc Imaging. 2021;14:1508–1519.
- Martinez-Naharro A, Kotecha T, Norrington K, et al. Native T1 and extracellular volume in transthyretin amyloidosis. JACC Cardiovasc Imaging. 2019;12:810–819.
- Porcari A, Fontana M, Canepa M, et al. Clinical and prognostic implications of right ventricular uptake on bone scintigraphy in transthyretin amyloid cardiomyopathy. Circulation. 2024;149:1157–1168.
- Rettl R, Wollenweber T, Duca F, et al. Monitoring tafamidis treatment with quantitative SPECT/CT in transthyretin amyloid cardiomyopathy. Eur Heart J Cardiovasc Imaging. 2023;24:1019–1030.
- Ioannou A, Fumagalli C, Razvi Y, et al. Prognostic value of a 6-minute walk test in patients with transthyretin cardiac amyloidosis. J Am Coll Cardiol. 2024;84:43–58.